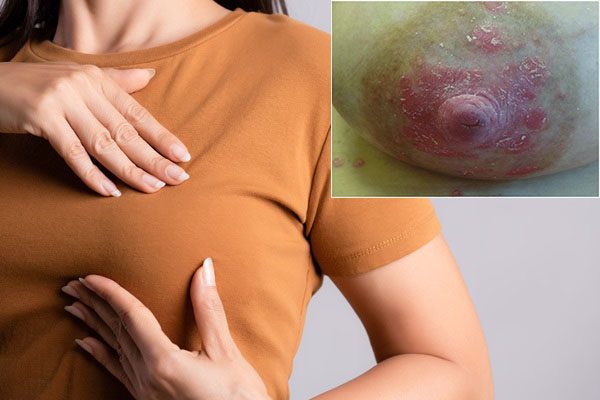
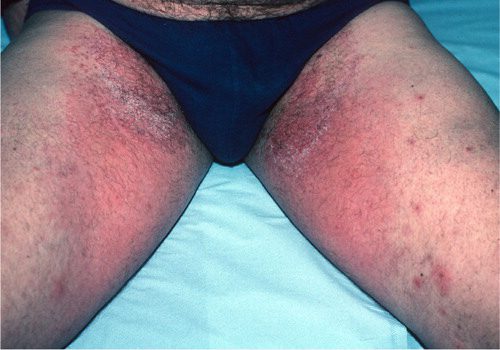
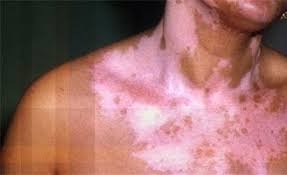
پسوریازیس (Psoriasis) یک بیماری با واسطه ایمنی در برخی از افراد دارای سابقه ژنتیکی است. این وضعیت به صورت اثرات التهابی روی پوست یا مفاصل، یا هر دو ظاهر میشود، و تأثیر زیادی بر کیفیت زندگی دارد.
پسوریازیس (Psoriasis) یک بیماری با واسطه ایمنی در برخی از افراد دارای سابقه ژنتیکی است. این وضعیت به صورت اثرات التهابی روی پوست یا مفاصل، یا هر دو ظاهر میشود، و تأثیر زیادی بر کیفیت زندگی دارد. هر چند که در حال حاضر درمانی برای پسوریازیس وجود ندارد، استراتژیهای مختلف درمان امکان کنترل پایدار علائم و نشانههای بیماری را فراهم میکند.
چندین کارآزمایی تصادفیسازی و کنترل شده (RCTs) به مقایسه اثربخشی درمانهای سیستمیک مختلف برای پسوریازیس در برابر پلاسبو پرداختند. با این حال، با توجه به تعداد محدودی از کارآزماییهایی که به مقایسه مستقیم آنها به صورت سربهسر (head to head) پرداختند منفعت نسبی این درمانها نامشخص باقی مانده است، به همین دلیل ما تصمیم به انجام یک متاآنالیز شبکهای (network meta-analysis) گرفتیم.
اهداف:
مقایسه اثربخشی و ایمنی عوامل سیستمیک معمول (آسیترتین (acitretin)، سیکلوسپورین (ciclosporin)، استرهای فوماریک اسید (fumaric acid esters)، متوترکسات (methotrexate))، مولکولهای کوچک (اپرمیلاست (apremilast)، توفاسیتینیب (tofacitinib)، ponesimod)، anti-TNF آلفا (anti-TNF alpha)، اتانرسپت (etanercept)، اینفلیکسیماب (infliximab)، ادالیموماب (adalimumab)، سرتولیزوماب (certolizumab))، anti-IL23.12 (آستکینوماب (ustekinumab)) anti-IL17 (سکوکینوماب (secukinumab)، ایکسیکیزوماب (ixekizumab)، برودالوماب (brodalumab))، anti-IL23 (guselkumab، tildrakizumab)، و سایر بیولوژیکها (الفاسپت (alefacept)، ایتولیزوماب (itolizumab)) برای بیماران مبتلا به پسوریازیس متوسط تا شدید و برای ارائه رتبهبندی این درمانها با توجه به اثربخشی و ایمنی آنها.
روش های جستجو:
ما پایگاههای اطلاعاتی زیر را تا دسامبر ۲۰۱۶ جستوجو کردیم: ثبت تخصصی گروه پوست در کاکرین، پایگاه ثبت مرکزی کارآزماییهای کنترل شده کاکرین (CENTRAL؛ Cochrane Central Register of Controlled Trials)، MEDLINE، Embase، و LILACS. همچنین ما پایگاه ثبت ۵ کارآزمایی و گزارشهای سازمان غذا و داروی امریکا (FDA) و آژانس دارویی اروپا (EMA) را جستوجو کردیم.
ما فهرست منابع مطالعات انتخاب شده و حذف شده را برای منابع بیشتر مربوط به RCTهای مرتبط کنترل کردیم. ما پایگاههای اطلاعاتی کارآزمایی مربوط به تعدادی از شرکتهای داروسازی را جستوجو کرده و خلاصهمقالات کنفرانس تعدادی از جلسات درماتولوژی را به صورت دستی جستوجو کردیم.
معیارهای انتخاب:
کارآزماییهای تصادفیسازی و کنترل شده (RCTs) مربوط به درمانهای سیستمیک و بیولوژیک بزرگسالان (بالای ۱۸ سال) مبتلا به پلاک متوسط تا شدید پسوریازیس یا آرتریت پسوریاتیک که پوست آنها از لحاظ بالینی مبتلا به پسوریازیس متوسط تا شدید تشخیص داده شده، در هر مرحله از درمان، در مقایسه با پلاسبو یا یک عامل فعال دیگر.
گردآوری و تحلیل دادهها:
۳ گروه متشکل از دو نویسنده مطالعه مروری بهطور مستقل انتخاب مطالعه، استخراج دادهها، ارزیابی «خطر سوگیری» (Bias)، و تجزیهوتحلیلها را انجام دادند. برای مقایسه درمانهای مطلوب و رتبهبندی آنها با توجه به اثربخشی (بر اساس اندازهگیری نمره شاخص منطقه و شدت پسوریازیس (PASI) 90) و قابلیت پذیرش آنها (اثرات جانبی جدی معکوس) ما دادهها را با استفاده از متاآنالیز دوتایی و شبکهای (NMA؛ pair-wise and network meta-analysis) ترکیب کردیم.
ما اطمینان شواهد به دست آمده را از NMA برای دو پیامد اولیه با توجه به GRADE، ارزیابی کردیم؛ ما شواهد را بسیار پایین، پایین، متوسط، یا بالا ارزیابی کردیم. در جایی که دادهها نامشخص بود یا از دست رفته بود با نویسندگان مطالعه تماس گرفتیم.
نتایج اصلی:
ما ۱۰۹ مطالعه را در مطالعه مروری خود انتخاب کردیم (۳۹۸۸۲ شرکتکننده تصادفیسازی شده، ۶۸% مرد، همگی در بیمارستان به کار گرفته شدند). میانگین کلی سن ۴۴ سال بود؛ میانگین کلی نمره PASI در ابتدای مطالعه ۲۰ بود (محدوده: ۵٫۹ تا ۳۹). اکثر این مطالعات با پلاسبو کنترل شدند (۶۷%)، ۲۳% مطالعات سر ـ به ـ سر (head-to-head) بوده، و ۱۰% از مطالعات چند بازویی دارای مقایسه کننده فعال و پلاسبو بودند. ما تمام درمانهای ذکر شده را در اهداف ارزیابی کردهایم (در مجموع ۱۹). در کل، ۸۶ کارآزمایی، کارآزماییهای چندمرکزی بودند (۲ تا ۲۳۱ مرکز). تمام کارآزماییهای انتخاب شده در این مطالعه مروری محدود به مرحله القا بودند (ارزیابی در کمتر از ۲۴ هفته پس از تصادفیسازی)؛ در واقع، تمام کارآزماییهایی که در متاآنالیز شبکهای انتخاب شدند، بین ۱۲ تا ۱۶ هفته پس از تصادفیسازی اندازهگیری شدند. ما اکثریت مطالعات (۱۰۹٫۴۸) را در معرض خطر بالای سوگیری ارزیابی کردیم؛ ۳۸ مطالعه در معرض خطر نامشخص، و ۲۳ مطالعه در معرض پایین ارزیابی شدند.متاآنالیز شبکهای در سطح کلاس نشان داد که تمام مداخلات (عوامل سیستمیک معمول، مولکولهای کوچک، و درمانهای بیولوژیکی) از لحاظ دستیابی به PASI 90 بهطور قابل ملاحظه ای موثرتر از پلاسبو بودند.
از لحاظ رسیدن به PASI 90، درمانهای بیولوژیک anti-IL17، anti-IL23.12، anti-IL23، و anti-TNF آلفا بهطور قابل توجهی موثرتر از مولکولهای کوچک و عوامل سیستمیک معمول بود. مولکولهای کوچک با احتمال بالاتری برای رسیدن به PASI 90 در مقایسه با عوامل سیستمیک معمول همراه بود.در سطح دارو، از لحاظ رسیدن به PASI 90، تمام عوامل anti-IL17 و guselkumab (یک داروی anti-IL23) بهطور قابل توجهی موثرتر از عوامل anti-TNF آلفا اینفلیکسیماب (anti-TNF alpha agents infliximab)، آدالیموماب، و اتانرسپت بود، اما موثرتر از سرتولیزوماب نبود. آستکینوماب برتر از اتانرسپت بود. تفاوت واضحی بین اینفلیکسیماب، آدالیموماب، و اتانرسپت وجود نداشت.
فقط یک کارآزمایی، اثربخشی اینفلیکسیماب را در این شبکه ارزیابی کرد؛ بنابراین، این نتایج باید با احتیاط تفسیر شوند. توفاسیتینیب (Tofacitinib) بهطور قابل ملاحظهای برتر از متوترکسات بود، و تفاوت واضحی بین هر یک از مولکولهای کوچک دیگر در مقابل درمانهای معمول وجود نداشت.
متاآنالیز شبکهای همچنین نشان داد که ایکسیکیزوماب، سکوکینوماب، برودالومب، guselkumab، سرتولیزوماب، و آستکینوماب در مقایسه با پلاسبو از لحاظ دستیابی به PASI 90 بیش از داروهای دیگر استبا توجه به اثربخشی (پیامد PASI 90) و پذیرش (پیامد SAE)، درمانهای بسیار موثر نیز در مقایسه با سایر درمانها SAE دارند، و به نظر میرسد که آستکینوماب، اینفلیکسیماب، و سرتولیزوماب تعامل بهتری از نظر اثربخشی و قابلیت پذیرش آن دارد.اطلاعات مربوط به کیفیت زندگی اغلب ضعیف گزارش شد و برای یک سوم از مداخلات وجود نداشت.
نتیجهگیریهای نویسندگان:
مطالعه مروری ما نشان میدهد که در مقایسه با پلاسبو، ایکسیکیزوماب بیولوژیک، سکوکینوماب، برودالوماب، guselkumab، سرتولیزوماب، و آستکینوماب بهترین انتخاب برای دستیابی به PASI 90 در افراد مبتلا به پسوریازیس متوسط تا شدید بر اساس شواهد متوسط تا بالا است. در سطح کلاس، درمانهای بیولوژیک anti-IL17، anti-IL23.12، anti-IL23، و anti-TNF آلفا همچنین بهطور قابلتوجهی موثرتر از مولکولهای کوچک و عوامل سیستمیک متعارف بودند. این شواهد NMA محدود به القای درمان است (پیامدها بین ۱۲ تا ۱۶ هفته پس از تصادفیسازی اندازهگیری شدند) و به اندازه کافی با بیماری مزمن مرتبط نیست.
علاوه بر این، تعداد کمی از مطالعات برای برخی از این مداخلات، و سن پایین (میانگین سن ۴۴ سال) و سطح بالایی از شدت بیماری (PASI 20 از خط پایه) ممکن است برای بیماران دیده شده در عمل بالینی روزانه معمول نباشد.یکی دیگر از نگرانیهای عمده این است که کارآزماییهای کوتاهمدت دادههای گزارش شده را مربوط به ایمنی اندک و گاهی ضعیف ارائه میدهند و بنابراین شواهد مفیدی برای ایجاد پروفایل خطر قابل اطمینانی را از درمانها ارائه نمیکنند. در واقع، تفاوت معنیداری در مداخلات ارزیابی شده و پلاسبو در رابطه با SAEها نیافتیم. متوترکسات بهنظر میرسد که بهترین پروفایل ایمنی را داشته باشد، اما از آنجایی که کیفیت شواهد بسیار پایین تا متوسط بود، ما نمیتوانیم از این رتبهبندی مطمئن باشیم. به منظور ارائه اطلاعات طولانیمدت در مورد ایمنی درمانهای انتخاب شده در این مطالعه مروری، ارزیابی مطالعات غیرتصادفی شده و گزارشهای پس از فروش که از سوی آژانسهای نظارتی نیز ارزیابی شود، ضروری خواهد بود.
با توجه به تحقیقات آینده، انجام کارآزماییهای تصادفیسازی شدهای که به مقایسه عوامل فعال به طور مستقیم بپردازند، هنگامی که شواهدی با کیفیت بالا درباره منفعت بر علیه پلاسبو یافت شود، ضروری هستند، از جمله کارآزماییهای سر ـ به ـ سر (head-to-head) درباره و در بین درمانهای سیستمیک متعارف و مولکولهای کوچک، و بین عوامل بیولوژیک (anti-IL17 در مقابل anti-IL23، anti-IL23 در مقابل anti-IL23.12، anti-TNF آلفا در مقابل anti-IL23.12). کارآزماییهای آینده همچنین باید تجزیهوتحلیل زیر گروهی سیستمیک انجام دهند (برای مثال ارزیابی بیماران بیولوژیک ساده، شدت پایه پسوریازیس، بروز آرتریت پسوریاتیک، و غیره). در نهایت، پیامد ارزیابی هماهنگی در کارآزماییهای مربوط به پسوریازیس مورد نیاز است، و محققان باید منافع میانمدت و بلندمدت و ایمنی مداخلات و ایمنی مقایسهای عوامل مختلف را بررسی کنند.