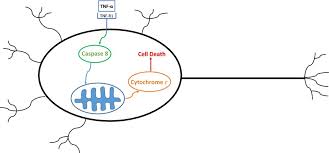
داروهای بیولوژیک نوع جدیدتری از داروها هستند که برای درمان پسوریازیس و آرتریت پسوریاتیک استفاده می شوند. این داروها قسمت هایی از سیستم ایمنی هدف قرار می دهند. بیولوژیک ها سرعت آسیب مفاصل را کم کرده و علائمی چون درد مفاصل، تورم و پوست فلسی را تسکین می دهند. پزشک معمولا وقتی سایر درمانها برای بیمار عمل نمی کند، درمان با بیولوژیک ها را شروع می کند. آنچه در زیر می آید نگاهی است به آخرین دستورالعمل آکادمی آمریکایی درماتولوژی در زمینه تجویز مهارکننده های TNF در درمان پسوریازیس است:
اصول عمومی مصرف مهارکننده های TNF:
عوامل ضد TNF (فاکتور نکروز دهنده تومور) در بیماران مبتلا به عفونت های فعال و جدی منع مصرف دارند.
انجام تست توبرکلوزیس در همه بیمارانی که قرار است تحت درمان با این عوامل قرار گیرند، الزامی است، زیرا گزارش هایی از فعالیت دوباره توبرکلوزیس در بیماران درمان شده با عوامل ضد TNF وجود دارد.
در بیماران تحت درمان با عوامل ضد TNF، واکسیناسیون با واکسن های زنده ممنوع است. در این بیماران باید از واکسن های غیرفعال از نظر بیولوژیکی یا واکسن های نوترکیب استفاده کرد. هرچند پاسخ ایمنی این واکسن ها باید مورد بررسی قرار گیرند.
از آنجا که ارتباطی میان درمان ضد TNF و بیماری دمیلینه کننده (مانند MS) وجود دارد، مهارکننده های TNF نباید در بیماران مبتلا به مالتیپل اسکلروزیس (MS) یا دیگر بیماری های دمیلینه کننده مورد استفاده قرار گیرند. بستگان درجه اول بیماران MS در معرض خطر ابتلا به این بیماری قرار دارند، بطوریکه این خطر در خواهر و برادر بین ۱۸ و ۳۶ درصد است. بنابراین شواهد قویا پیشنهاد می کنند که مهارکننده های TNF نباید در افراد فامیل درجه اول بیماران مبتلا به MS مورد استفاده قرار گیرد.
با توجه به گزارش های موجود در زمینه بروز و بدتر شدن نارسایی مزمن قلبی در بیماران درمان شده با مهارکننده های TNF، باید احتیاط های لازم در این زمینه صورت گیرد. در این زمینه توصیه می شود بیمارانی که طبق طبقه بندی انجمن قلب نیویورک، در کلاس ۳ یا ۴ نارسایی مزمن قلبی قرار دارند، نباید از مهارکننده های TNF استفاده کنند. بیمارانی که در کلاس ۱ یا ۲ هستند، باید در ابتدا تحت تست اکوی قلبی قرار گیرند. اگر کسر جهشی این بیماران کمتر از ۵۰ درصد است، درمان با مهارکننده های TNF ممنوع است.
فعال شدن دوباره هپاتیت B پس از درمان با مهارکننده های TNF گزارش شده، بنابراین در کار بالینی مناسب، بیماران باید از نظر ابتلا به عفونت هپاتیت B غربالگری شوند.
واکنش های متوسط دردناک در محل تزریق گزارش شده است. گزارش های نادری از عفونت های جدی (مانند سل و عفونت های فرصت طلب) و بدخیمی ها دیده شده است. گزارش های نادری از عوارض جانبی وابسته به دارو و برگشت پذیر، شامل لوپوس بدون عوارض کلیوی یا سیستم مرکزی عصبی، سیتوپنی، مالتیپل اسکلروزیس و حمله جدید نارسایی مزمن قلبی نیز منتشر شده است.
انواع داروهای مهارکننده های TNF:
درحال حاضر چند نوع داروی بیولوژیک موجود است که هر نوع از آن ها ، بر روی ملکول خاصی تاثیر می کنند. این داروها عبارتند از:
داروهائی که بر روی TNF اثر می کنند : این نوع داروها بر روی مولکولی به نام (Tumor Necrosis Factor(TNF اثر می کنند و به بلوک کنند های TNF یا داروهای anti TNF نامیده می شوند. این داروها برای درمان آرتریت روماتوئید ، آرتریت کودکان ، آرتریت پسوریاتیک و اسپوندیل آرتریت آنکیلوزانت مصرف می شوند. این داروها عبارتند از:
اتانرسپت (Etanercept)
اینفلکسی مب Infliximab)
آدالی مومب (Adalimumab)
گولی مومب (Golimumab)
سرتولیزو مب پگول (Certolizumab Pegol)
داروهائی که بر روی Interlukin-1 اثر می کنند: آناکینرا (Anakinra)
داروهائی که بر روی Interlukin-6 اثرمی کنند: توسیلی زومب (Tocilizumab)
دارهائی که لنفوسیت های B را از بین می برد: ریتوکسی مب (Rituximab)
داروهائی که از فعال شدن لنفوسیت های T جلوگیری می کنند: آباتاسپت (Abatacet)